In attesa della pubblicazione della lista di equivalenza dei medicinali veterinari di cui all’articolo 25, comma 4, del d.lgs 218/2023 che adegua la normativa nazionale alle disposizioni del Regolamento Ue 2019/6, la sostituzione in farmacia del farmaco prescritto dal veterinario «è consentita soltanto nei casi previsti dall’articolo 25, comma 2, del decreto medesimo. In questa fase transitoria, nel sistema informativo della tracciabilità è stata mantenuta la notifica di avvenuta sostituzione da parte del farmacista», che sarà eliminata con l’arrivo della lista ministeriale. Lo precisa la circolare del ministero della Salute (datata 8 febbraio) che detta le indicazioni operative per l’applicazione delle misure disposte dal decreto, in vigore dal 18 gennaio.
Per quanto concerne la prescrizione, in particolare, il Ministero ricorda che l’articolo 28 del decreto fissa la validità della ricetta veterinaria non ripetibile in 30 giorni dalla data di rilascio e in 6 mesi la validità della ricetta veterinaria ripetibile, con utilizzo per un massimo di dieci volte. «Con l’entrata in vigore del decreto quindi» avverte la circolare «decade la ricetta in triplice copia non ripetibile e di conseguenza tutti i medicinali autorizzati con la ricetta in triplice copia non ripetibile si intendono autorizzati con la ricetta non ripetibile. Il sistema informativo della tracciabilità ha recepito dal 18 gennaio scorso le modifiche, mentre gli stampati di tali medicinali – inclusi quelli autorizzati con procedura centralizzata – saranno aggiornati alla prima variazione dell’Aic che abbia impatto sugli stessi, senza la necessità di presentare una variazione ad hoc».
Tra le novità di rilievo del Regolamento Ue, anche l’Introduzione di medicinali veterinari da altri Stati Ue l’importazione da Paesi terzi. L’articolo 30 del d.lgs, chiarisce il Ministero, definisce le procedure correlate, riassunte nella circolare in una tabella esemplificativa che chiarisce i casi in cui l’azienda deve richiedere una nuova autorizzazione oppure è sufficiente una notifica e quelli in cui il veterinario può prescrivere sotto la propria responsabilità
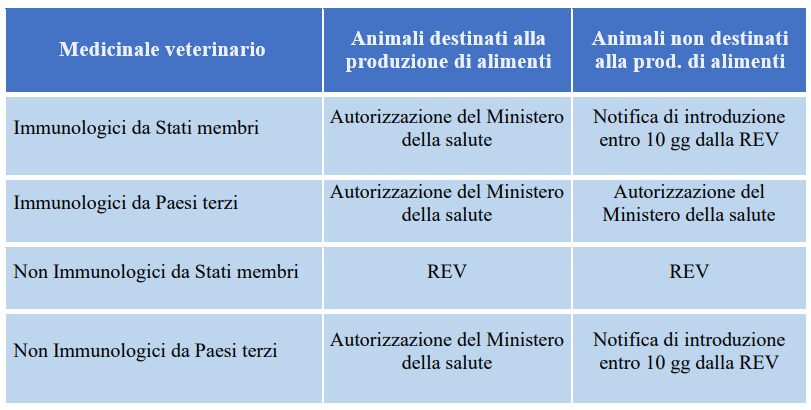
«Relativamente alla notifica (riguardante l’introduzione di un medicinale da altro Stato Ue, ndr), al momento si ritiene sufficiente la presenza nel sistema di una Rev per “Farmaco estero”», che verrà implementata successivamente.
Infine, per quanto riguarda l’attività di distribuzione all’ingrosso, la circolare ricorda che all’articolo 17 il decreto 218/2023 impone alla persona designata come responsabile del magazzino non soltanto il possesso della laurea in Farmacia, Ctf o Chimica industriale, ma anche che svolga «attività a carattere continuativo nella sede indicata nell’autorizzazione, con un orario compatibile con le necessità derivanti dalle dimensioni dell’attività di distribuzione espletata». La compatibilità di tale ruolo con quello di farmacista in parafarmacia, quindi, dipende dal rispetto di quanto dispone il dm 19 ottobre 2012, che richiede agli esercizi di vicinato autorizzati alla vendita di farmaci senza ricetta «la presenza per tutto l’orario di apertura di uno o più farmacisti, abilitati all’esercizio della professione e iscritti al relativo ordine professionale». Pertanto, conclude la circolare, «i due ruoli sono compatibili qualora le suddette attività vengano espletati in orari non sovrapponibili. L’organizzazione di dette attività deve essere indicata nel documento di qualità di cui al Regolamento di esecuzione 2021/1248, tenuto a disposizione delle autorità territorialmente competenti».