Il nuovo sistema comunitario di tracciatura del farmaco, da oggi operativo in 31 Stati dello Spazio economico europeo, lascerà fuori Italia, Belgio e Grecia fino al 2025, in virtù della dilazione che Bruxelles ha concesso ai Paesi già forniti di propri sistemi anticontraffazione. Tuttavia, qualora Roma volesse optare «per l’immediata operatività della tracciatura europea anche sul nostro territorio, le aziende produttrici italiane sono già pronte da tempo grazie all’impegno profuso negli ultimi tre anni». E’ quanto scrivono Farmindustria, Assogenerici e Aip (l’Associazione degli importatori paralleli) nel comunicato congiunto diffuso ieri in concomitanza con la presentazione, a Bruxelles, del nuovo sistema di identificazione. Un’impalcatura informatica, ricorda la nota, che «collegherà duemila aziende farmaceutiche, circa seimila grossisti, 140mila farmacie, cinquemila farmacie ospedaliere e tutti gli operatori autorizzati a dispensare farmaci nello spazio economico europeo».
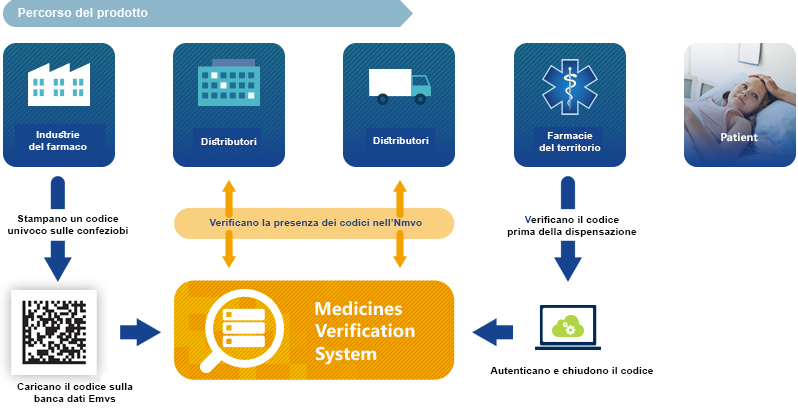
L’architettura contempla un database europeo, chiamato Emvs (European medicines verification system), collegato in rete alle banche dati nazionali (Nmvs, National medicines verification system) dei Paesi partecipanti. Le procedure di verifica seguono il cliclo di filiera: le aziende produttrici caricano in uscita sull’Emvs i codici univoci delle confezioni, tipo datamatrix; i distributori intermedi verificano all’ingresso, nella banca dati Nmvs del proprio Paese, che i codici siano genuini le farmacie, all’atto della dispensazione al banco, ripetono la verifica (sempre nell’Nmvs nazionale) e chiudono il codice, certificandone l’uscita definitiva dal ciclo distributivo (senza possibilità di rientro).
Come detto, l’Italia manterrà il proprio sistema di tracciatura (basato sulle fustelle adesive) fino al 2025, ma la filiera farmaceutica ha già compiuto i primi passi per costituire l’Nvmo (National medicines verification organization) che a sua volta dovrà gestire l’Nvms, cioè la banca dati nazionale. A tale scopo, un anno fa le sigle del comparto (Farmindustria, Assogenerici, Federfarma, Assofarm, Adf e Federfarma Servizi) avevano firmato un protocollo d’intesa che definiva quote e impegni di ciascuna e assecondava il desiderio degli industriali di provare ad anticipare di qualche anno (al 2020 o ’21) il passaggio alla tracciatura europea. Motivi prettamente economici: le aziende italiane fanno molto export, quindi sono già attrezzate per stampare le confezioni con codice datamatrix; la targatura italiana (basata su fustelle adesive realizzate dal Poligrafico) costa parecchio alle imprese, il sistema europeo invece sarebbe molto più economico perché i codici sono stampati sulle scatolette e non hanno strati adesivi.
Ecco dunque il motivo per cui, nel comunicato congiunto, Farmindustria e Assogenerici insistono sul fatto che in caso di anticipazione le aziende farmaceutiche sarebbero già pronte. Ma le farmacie? «La transizione al nuovo sistema andrà gestita con la dovuta attenzione» è la risposta del presidente di Promofarma, Nicola Stabile «ma siamo comunque coscienti che il passaggio alla tracciatura europea è un processo importante perché rappresenta la nuova frontiera della lotta alla contraffazione». In quest’ottica, è il parere di Stabile gli adeguamenti hardware e software che si renderanno necessari (scanner 2D e aggiornamenti dei gestionali) non generano preoccupazione: «A occhio e croce» osserva «oggi meno della metà delle farmacie italiane dispone di lettori capaci di leggere i codici datamatrix (in Francia due su tre, ndr), ma non è questo il problema». La vera sfida, piuttosto, saranno le ricadute sull’attività al banco: se per ogni confezione il farmacista deve leggere il codice, attendere che il sistema ne verifichi la presenza sulla banca dati nazionale, chiuderlo e dispensare il farmaco, il rischio di code e imbottigliamenti al banco cresce a dismisura. E si tratta di operazioni che non possono essere procrastinate, perché – come detto – i codici sono stampati sulle confezioni dunque non è possibile togliere il fustello, attaccarlo da qualche parte e rinviare la verifica online a un periodo più tranquillo della giornata. «E’ vero» ammette Stabile «il problema c’è e lo stiamo studiando. La necessità è quella di adeguare le disposizioni alla quotidianità del lavoro in farmacia, nel rispetto delle esigenze e della privacy dei pazienti. Ci aspettiamo che nel recepimento italiano vengano contemplate clausole di salvaguardia, come già accade per la ricetta elettronica, perché in ogni caso la prima preoccupazione dev’essere quella di salvaguardare la dispensazione».